新薬 開発 流れ

データが変える薬剤の価値 リアルワールドデータが製薬企業にもたらすもの Answersnews

研究開発について 研究開発 デ ウエスタン セラピテクス研究所
Q Tbn 3aand9gctppz3gsdrtzcl37iu Klyvhqng18qmyij7z69lhyeyayhathdc Usqp Cau

進化を続ける製薬業界とcroの存在意義 イーピーエス株式会社採用情報
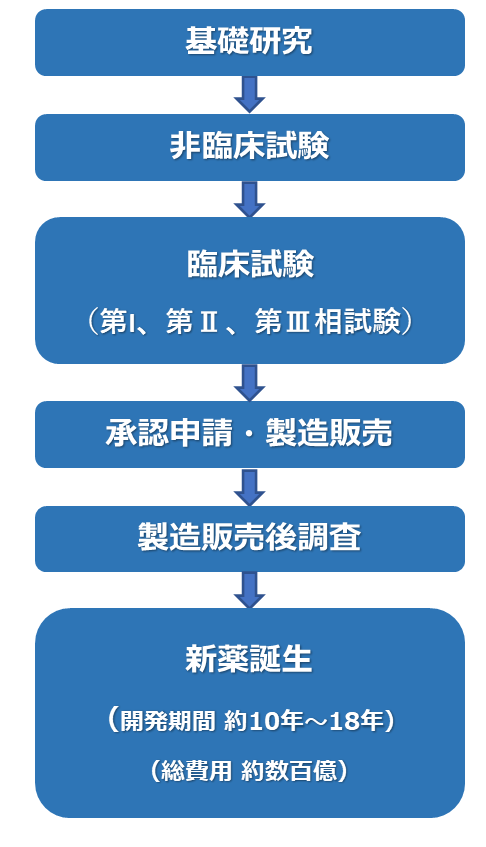
医薬品開発の流れ

安全創薬 メンバー
① 日本人患者の新薬アクセスの改善 (国民の健康、厚生) ② 研究開発の場としての日本の活性化 (研究開発、教育、競争力) ③ (日本の)製薬企業の支援 (雇用、ノウハウ、競争力) • 医薬品等の審査プロセス等に改善すべき点はまだある。.

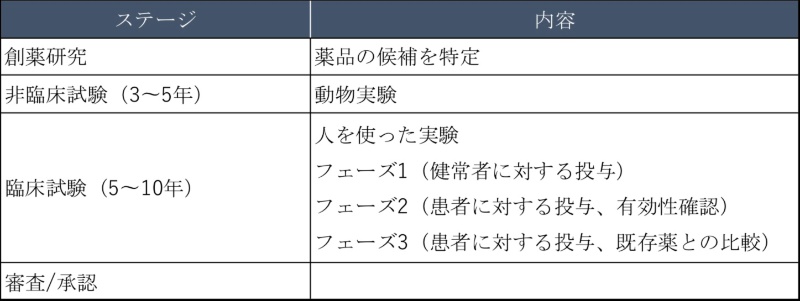
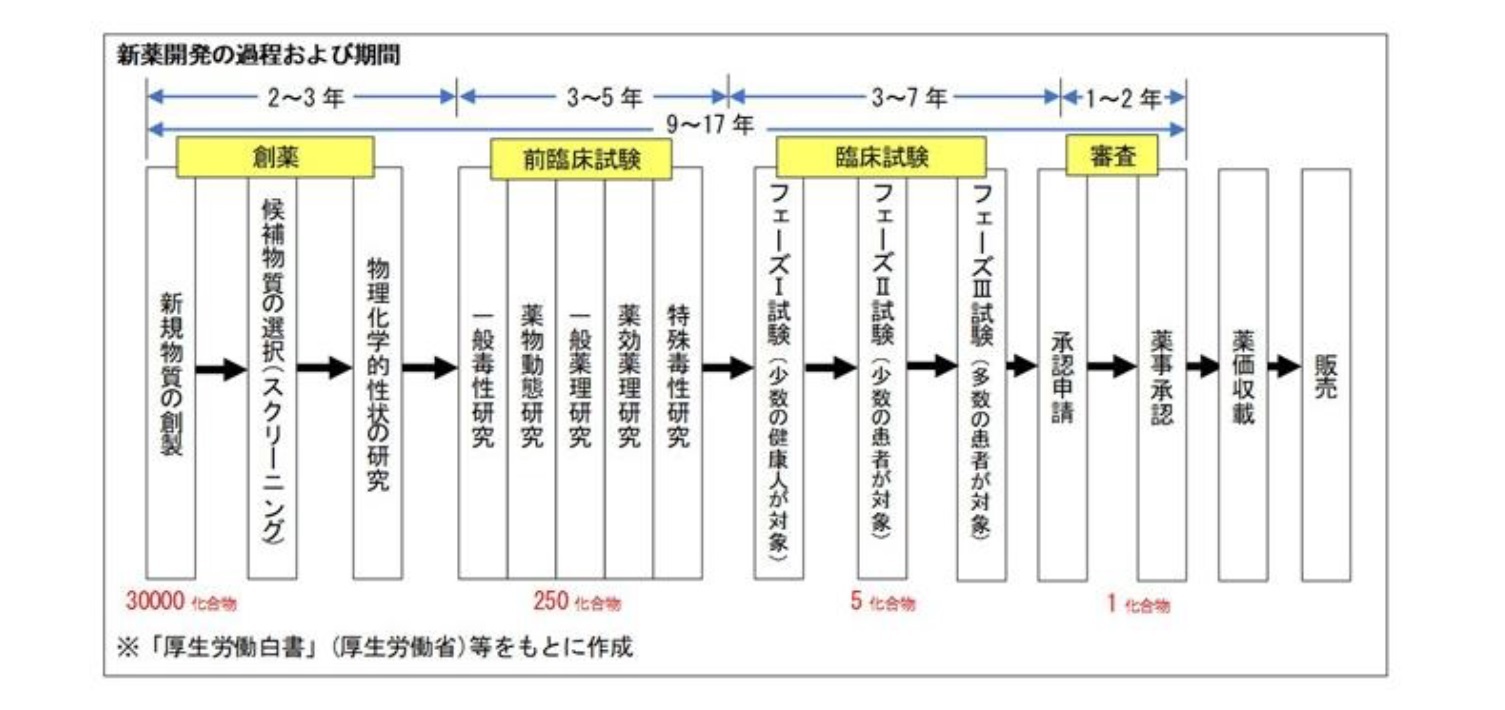
新薬 開発 流れ. 薬品開発の羅針盤により,製品化への成功は疑う余 地がなくなった.実際,治療の主流となっている医 薬品の数多くは,この時期に開発,発売された.当 時は,他社に先駆け革新的新薬を開発することに焦 点があてられ(firstintheclass),その過程で開発が. 開発ラグ :当該年度に国内で新規承認申請された新薬について、米国における申請時期との差の中央値 審査ラグ :当該年度(米国は暦年)における日米間の新薬の新規承認された総審査期間(中央値)の差 ドラッグ・ラグ :開発ラグと審査ラグの和 (注1). 医薬品の開発の基本的な流れ 医薬品のモトとなる新規物質の合成・発見 新規物質の有効性と安全性の研究(動物が対象) ヒトを対象とした 有効性と安全性 のテスト 企業から厚生労働省への承認申請と (独)医薬品医療機器総合機構による審査.
医薬品の研究開発費は増加傾向にある 社当たりの研究開発費: 621億円(04年)⇒1,414億円(17年) 新薬の上市に必要な開発費(海外):約1,700億円(14年) ※出典:有価証券報告書に基づき医薬産業政策研究所により作成(大手製薬10社). 参考:医薬品の開発の流れ 基礎研究 応用研究(少なくとも10年以上を要する) 産業応用 (実用化) 病気の 本態解明 ヒット 化合物 創薬標的 タンパク質 リード 化合物 医薬品 候補 医薬品 製薬企業と共同研究 (ライセンスアウト) ターゲットタンパク研究. 新薬開発の道のり・臨床試験(治験)の流れ 新しい薬を創るためには様々な試験を行い、有効性や安全性を評価する必要があります。 臨床試験(治験)とは、基礎研究、非臨床試験などの研究過程を経て、薬の候補が実際に人に役立つかどうかを確認する.
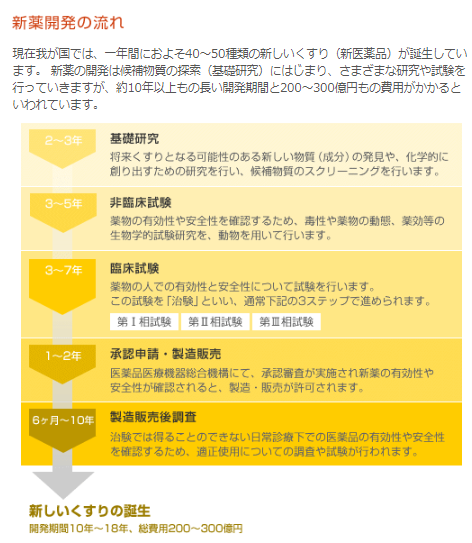
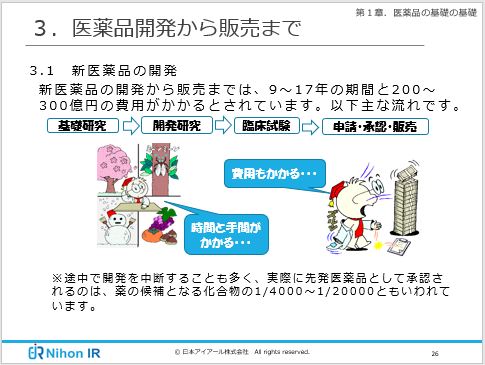
> 医薬品の創り方と開発から販売までの流れ > 医薬品の臨床試験(治験)の流れ 新薬の開発と言えども人への実験で未確認の物質を試すことなど絶対にあってはならないことです。. ⑥ 国際共同治験を活用した新薬開発の流れ ⑦ 日米(欧)における治験実施期間の比較 ⑧ 治験相談の実施状況(平成18年度) ⑨ 欧米で初めて承認されてから我が国で申請されるまで の期間 4 承認審査の段階 ① 機構における承認審査業務の概要. 以上のように基礎研究から製造・販売まで、くすりの開発には長い期間と多くの費用が必要で、新薬の 開発期間は約10年~18年、数百億円以上 といわれる。 また、基礎研究で探した新薬候補が実際に発売できる確率は 2万~3万分の1 といわれ、開発は年々難しさを増している。.
2:日本企業の新薬開発力(1) 日本企業の新薬創出の効率は高い 欧米 日本 出典:Annual Report(11)を基に1$=80円で換算、有価証券報告書(11) 社名 研究開発費(億円) Pfizer 7,290 Novartis 7,666 Merck 6,773 社名 研究開発費(億円) 武田 2,819 アステラス 1,8 第一三共 1,851. 理系大学院生の中で人気の職業と言えば「研究職」。 特に製薬会社の研究職は人気です。 新薬を作る研究職なんてロマンがあっていいじゃないですか。自分が携わった薬が世に出て患者さんの病気を治していくなんて、夢があっていいじゃないですか。 そして「開発職」も人気です。 臨床. 新薬の開発に携わる薬剤師の仕事として、新薬の生まれ方や、製薬会社での部門、転職シーンなどについて分かりやすく説明します。 新薬の誕生、とくに研究や開発に携わる仕事に対して、憧れや興味を持っている方の中には、 「でも実は、どんな仕事をしているのかイマイチ理解できてい.
医療機器を開発するにあたって どのようなものを医療機器と呼ぶのか? 医療機器を開発するとはどういうことか? 医療機器を上市するためにはどうしたらいいか? 勝手に作って売ってもいいのか?. るところであり、新薬開発原資の安定的な確保のため、新薬創出・適応外薬解消等促進加 算 ※ の維持・制度化が喫緊の課題である。 ※新薬創出・適応外薬解消等促進加算の適用要件(以下を満たすこと) イ後発品が収載されていない(又は収載から15. 新薬開発の流れ 現在我が国では、一年間におよそ40~50種類の新しいくすり(新医薬品)が誕生しています。 新薬の開発は候補物質の探索(基礎研究)にはじまり、さまざまな研究や試験を行っていきますが、約10年以上もの長い開発期間と0~300億円もの.
特に医薬品開発に携わる方達は同じような危機感を持たれている方もおられるのではないでしょうか。 そこで今日は啓発も兼ねて、 医薬品の承認申請から薬価収載されて販売開始するまでの「一般的な」流れについて、簡単に見ていきたい と思います。.

製造販売承認の流れ 再生医療製品事業 株式会社ジャパン ティッシュ エンジニアリング J Tec
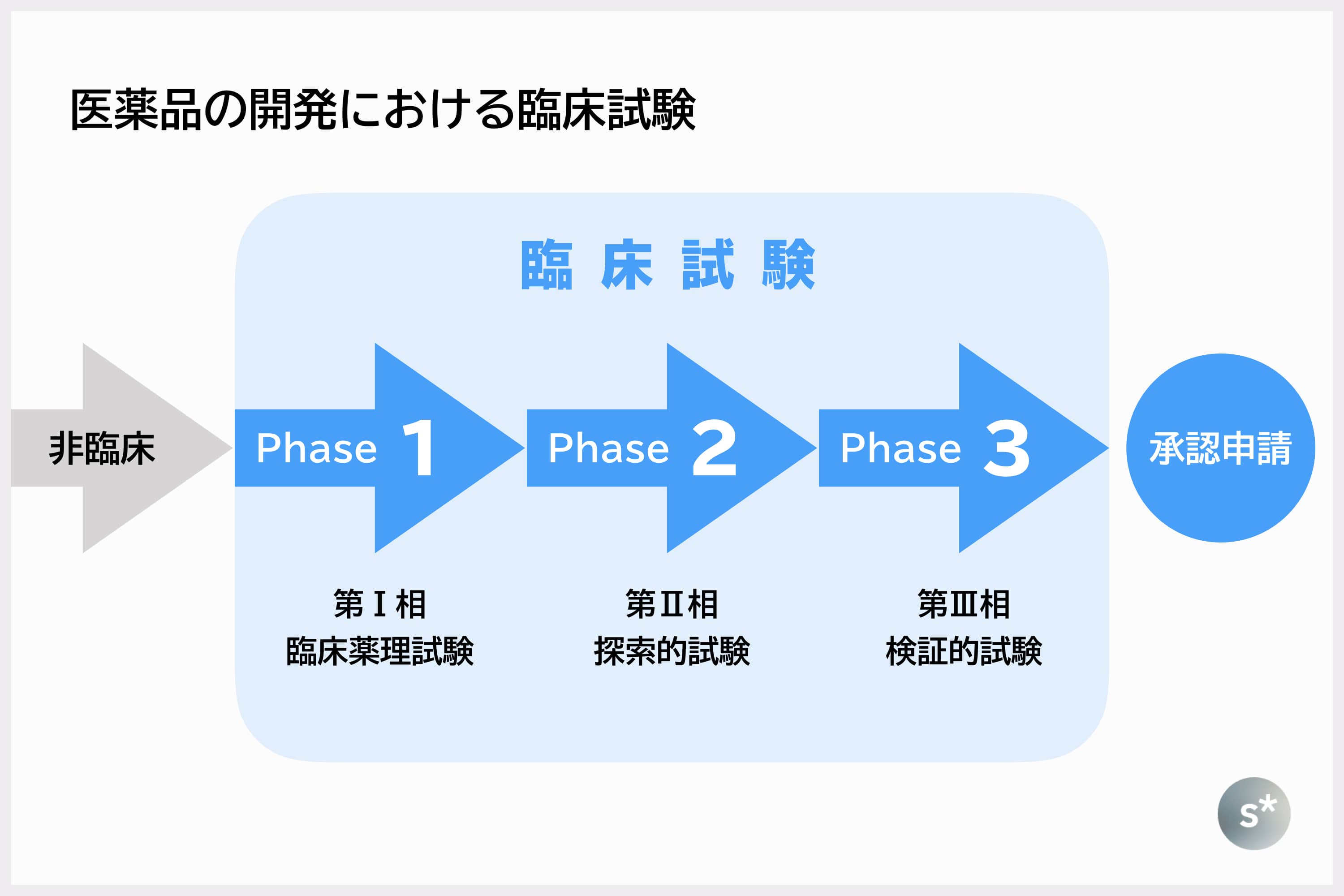
ドラッグラグ 医薬品開発における2つの ラグ を解説 Starnote

創薬 探索臨床研究コアセンター トランスレーショナルリサーチ部門 東北大学大学院医学系研究科附属 創生応用医学研究センター
Http Www Fpmaj Gr Jp Documents 29yakuseisetumeikai Pdf

臨床研究モニター 株式会社リニカル

創薬研究職 臨床開発職 About Us エーザイ株式会社 18 Recruiting Website

Mr職 研究開発職 生産職 仕事紹介 あすか製薬株式会社 Recruit21
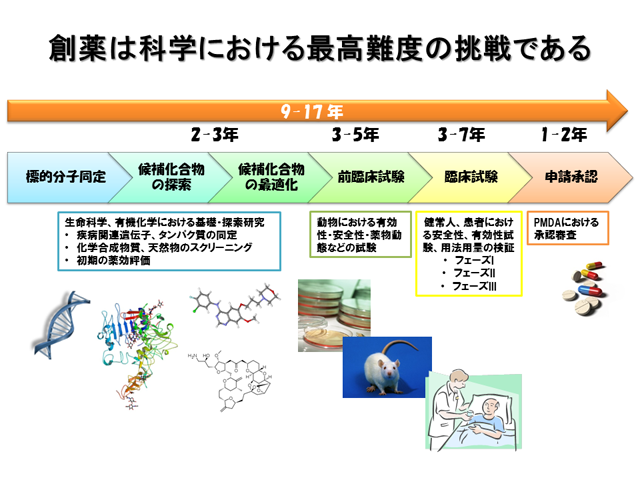
創薬 って何 達人に訊け 中日新聞web
製薬企業における新薬開発の流れ 莫大な研究開発費と期間が必要です
1

マイクロドーズ臨床試験の受託を開始 ニュース 積水メディカル株式会社

進化を続ける製薬業界とcroの存在意義 イーピーエス株式会社採用情報
Oncology領域のphase1試験について考えてみる 臨床開発 はるきちのブログ

日本ジェネリック株式会社 ジェネリック医薬品をもっと良く知っていただくために ジェネリック医薬品は なぜ安いの

シミックホールディングスの企業研究 製薬業界の転職サイト Answers アンサーズ

ジェネリック医薬品と薬剤師
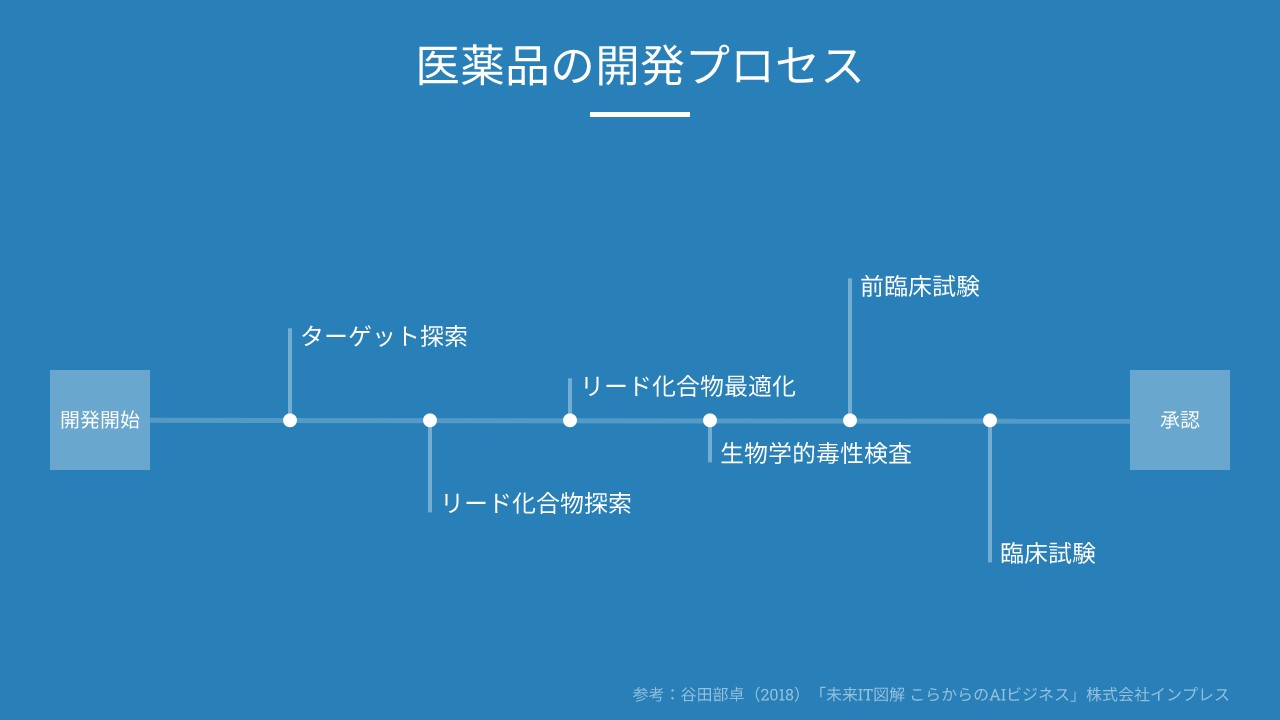
Aiは創薬の課題を解決できるのか Aiが創薬に及ぼす影響 Ai専門ニュースメディア Ainow
Www Mhlw Go Jp Shingi 10 04 Dl S0421 4c 0002 Pdf

医薬品の特許 製薬会社が独占販売できる期間は10年程度

Smoの役割と主な業務 日本smo協会
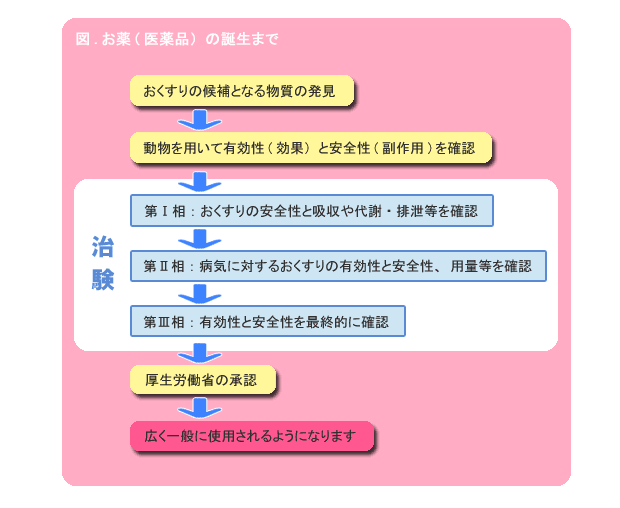
治験の実施プロセスとインフォームドコンセント

Q33 1つのくすりを開発するのに どれくらいの年月がかかりますか くすりについて 日本製薬工業協会

医薬品ができるまで 日本新薬ってどんな会社 日本新薬新卒採用ページ 日本新薬株式会社
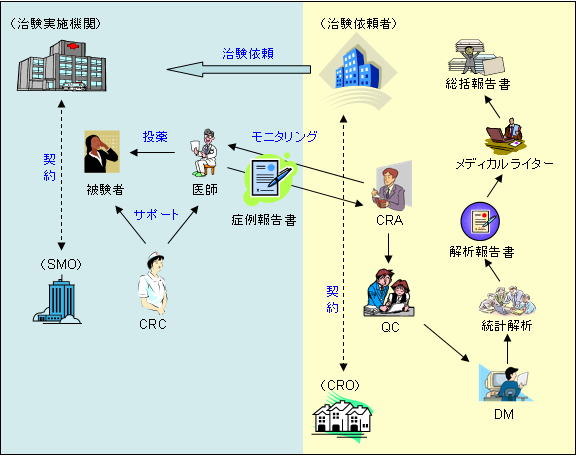
医薬品 医療機器の研究 開発 ポータルサイト 治験 臨床開発 臨床統計 Beagle Hc

Cro Smoへの就職と業界動向 薬剤師 薬学部生のインターン 就業体験情報ならめでぃしーんねっと22
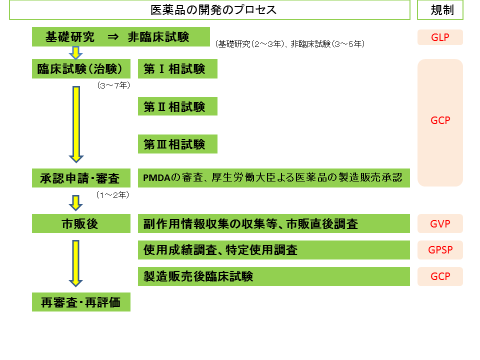
医薬品の開発プロセス 治験 発ケン 広島県 広島県

治験スタートアップbuzzreach代表に聞くcovid 19の治療薬とワクチンの開発状況についてのインタビュー News 株式会社kvp
Q Tbn 3aand9gcrbvtiyalvbd7bzxaqkzvmboxhg43ob4nvcudm5ieqy84tqmr T Usqp Cau

薬ができるまで メディカルボランティアセンター

製造販売承認の流れ 再生医療製品事業 株式会社ジャパン ティッシュ エンジニアリング J Tec
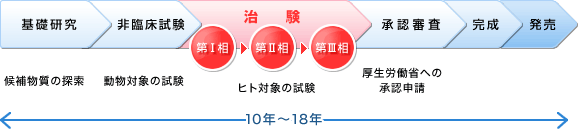
製薬企業における新薬開発の流れ 莫大な研究開発費と期間が必要です

あるnpoの挑戦 障壁だらけの 新薬開発 は オープン クラウドソースで加速するか Wired Jp

新薬開発の成功率は くすりの知識10ヵ条 第2条 一般社団法人 くすりの適正使用協議会
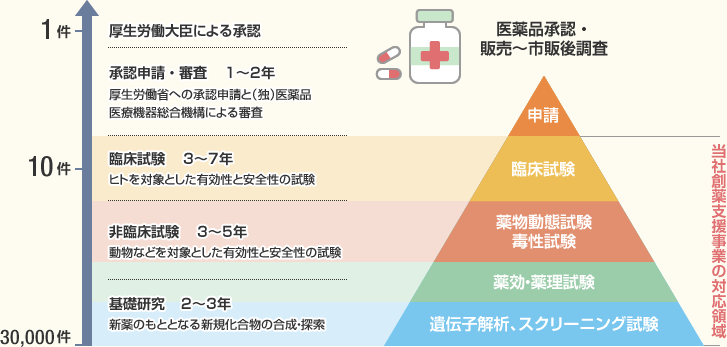
創薬支援事業 積水メディカル株式会社 新卒採用サイト

Iist World Forum No01 0768 J 医薬品産業が新たな成長産業となるために 永井 健寛

Dr 株式会社lttバイオファーマ
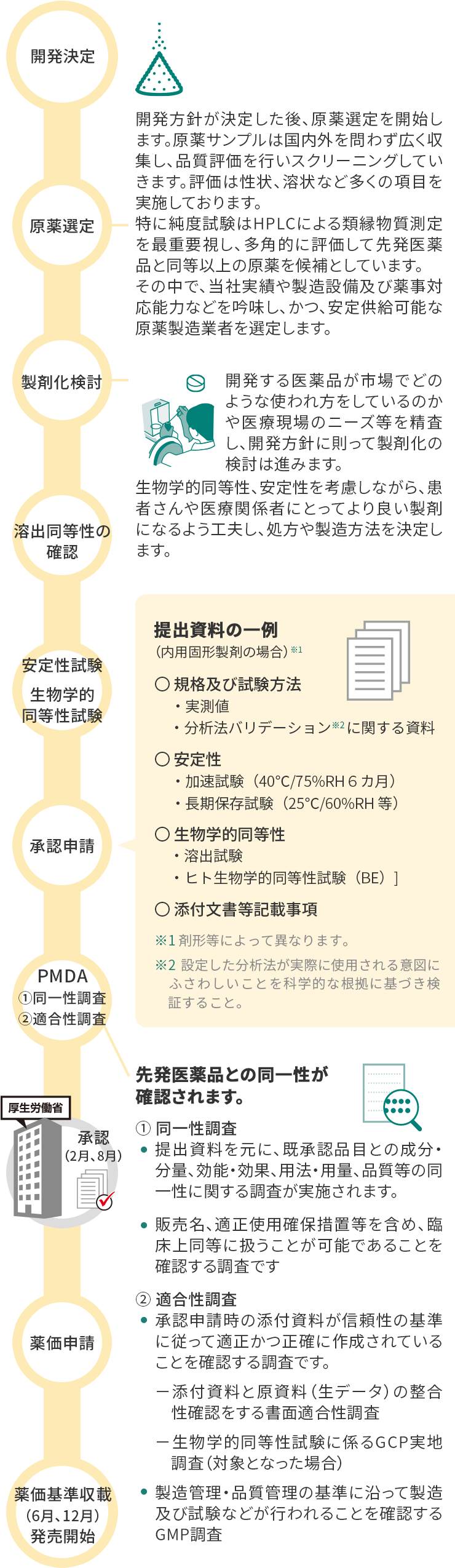
サワイジェネリック 開発への取り組み 沢井製薬
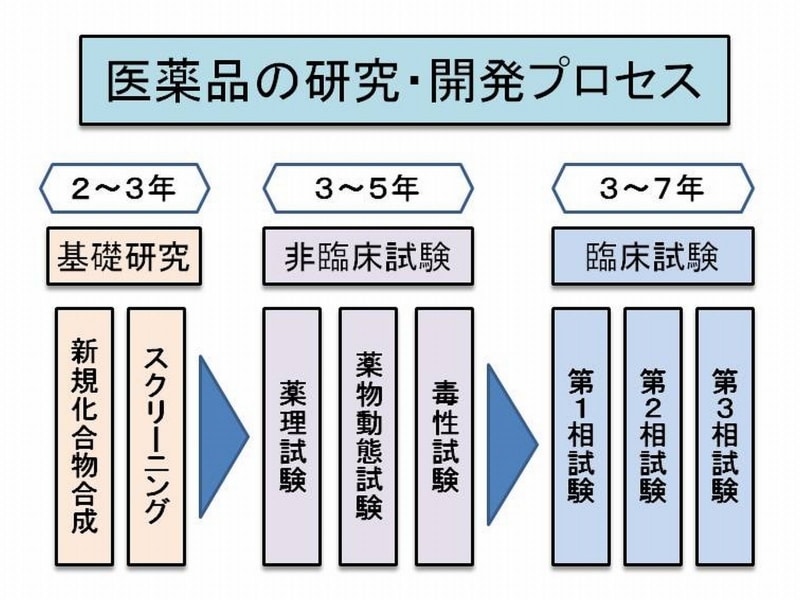
医薬品の研究開発から流通まで 基本と最近の課題 Mrの転職 All About
Www Mhlw Go Jp File 05 Shingikai Daijinkanboukouseikagakuka Kouseikagakuka Pdf

医薬品情報学 研究室紹介 研究 慶應義塾大学 薬学部 薬学研究科
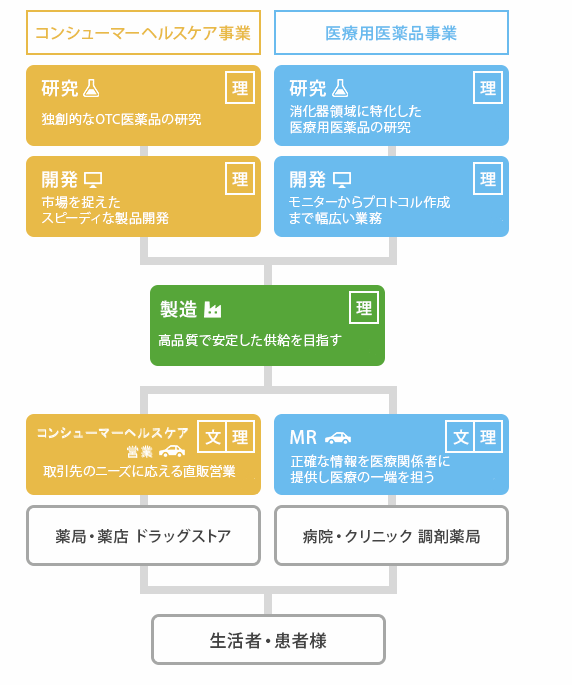
職種相関 採用情報 ゼリア新薬工業
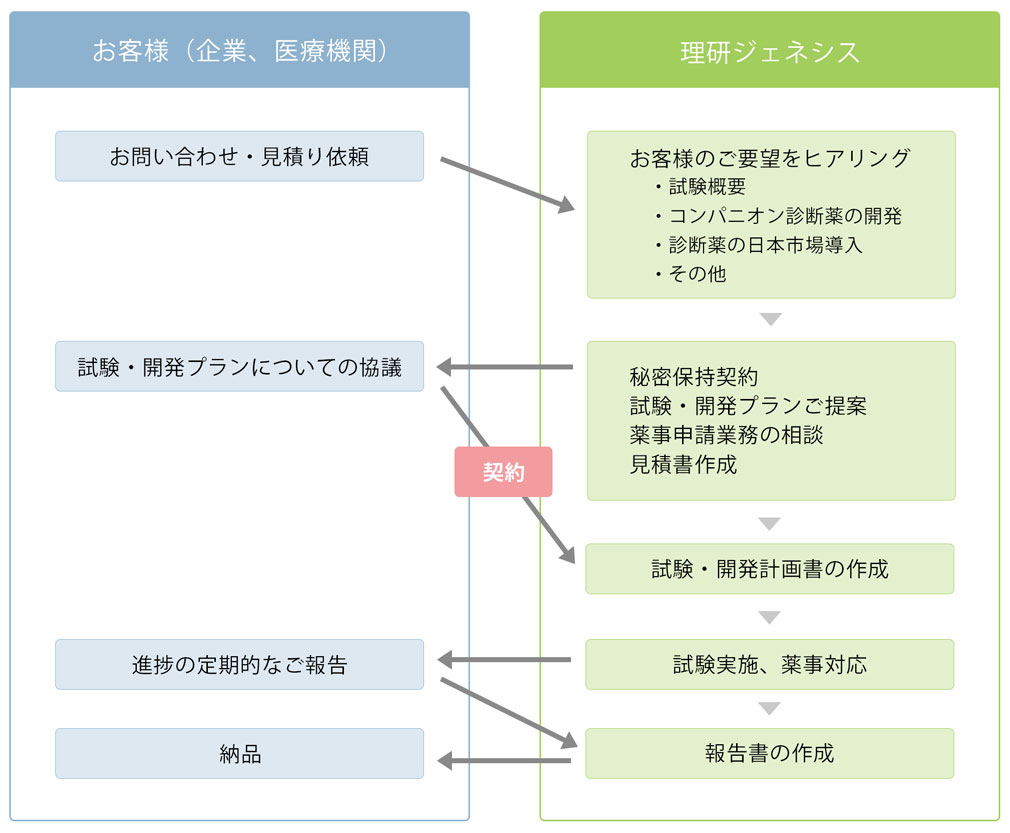
医薬品開発支援

研究開発 創薬研究 の流れ 研究開発 エーザイ株式会社
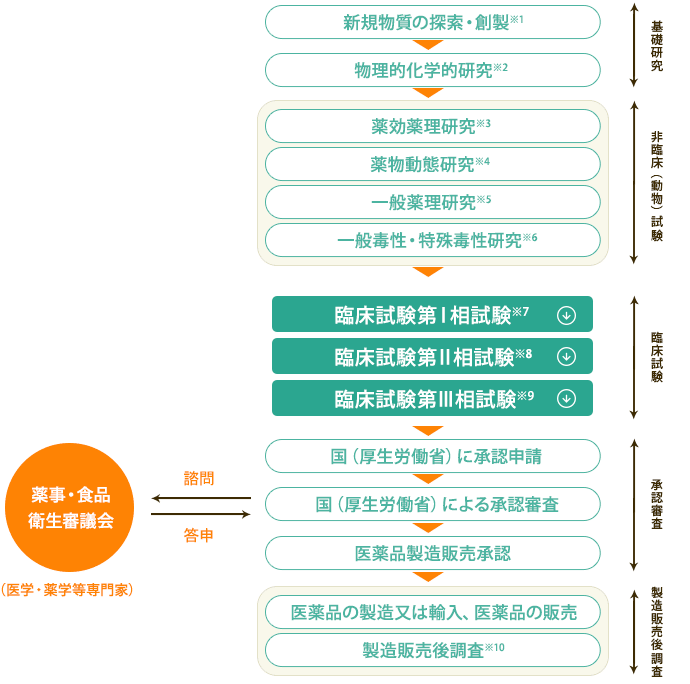
治験の3つのステップ 一般の方へ 群馬大学医学部附属病院 臨床試験部

くすりができるまで 日本smo協会
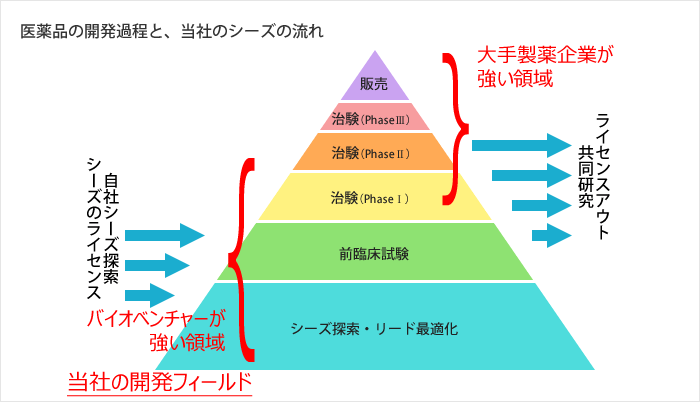
ビジネスモデル Sbiバイオテック

くすりができるまで 日本smo協会
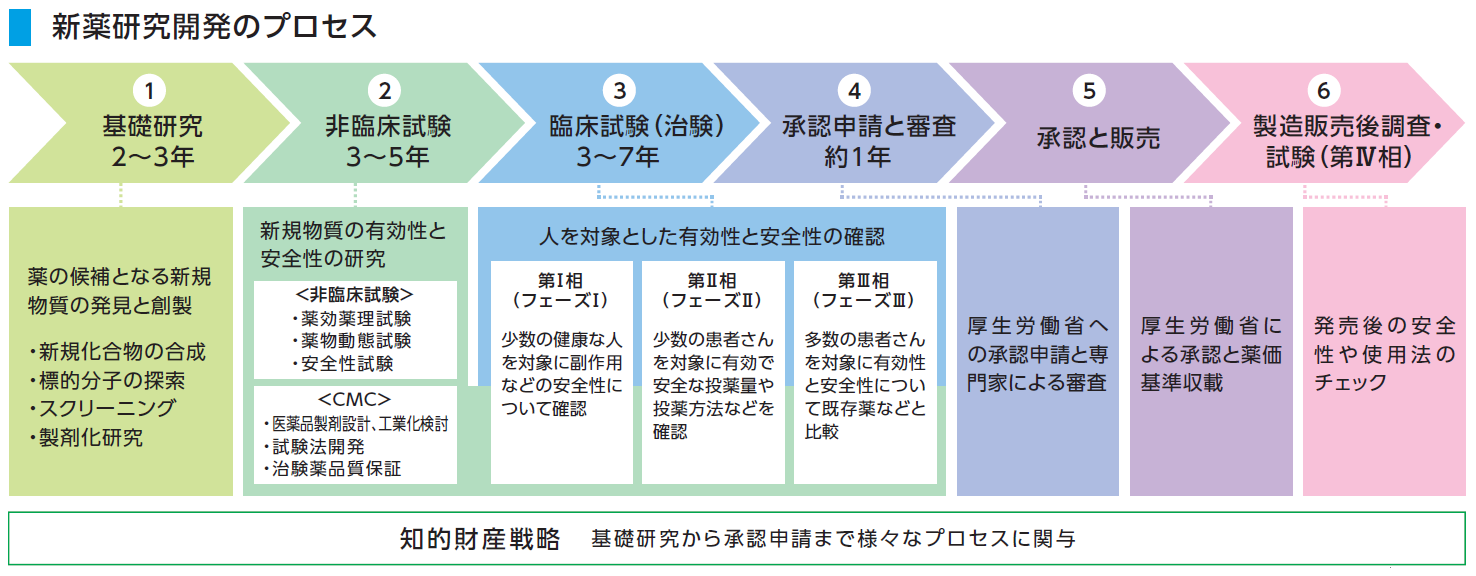
新薬研究開発のプロセス 研究開発 生化学工業株式会社
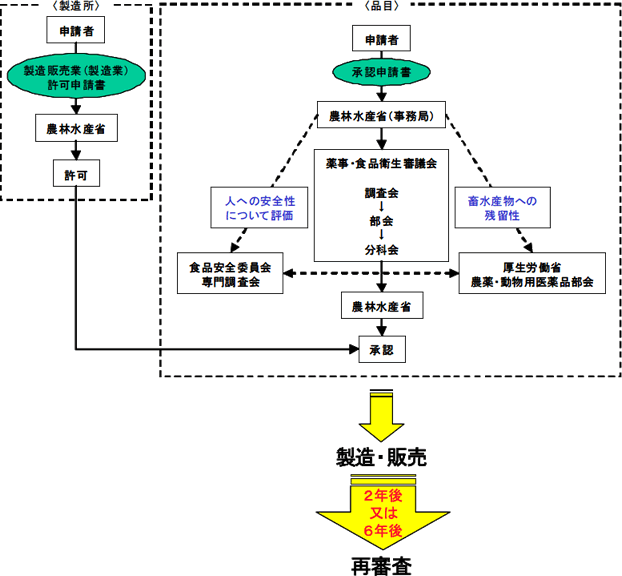
開発の流れ 公益社団法人日本動物用医薬品協会

新薬の薬価はどう決まる Answersnews Plus

受託サービスの流れ バイオ医薬品安全性試験サービス バイオ医薬品開発支援サービス 遺伝子医療 タカラバイオ株式会社
2

イーピーエス株式会社 Equitystory Ir担当者インタビュー Vol 22
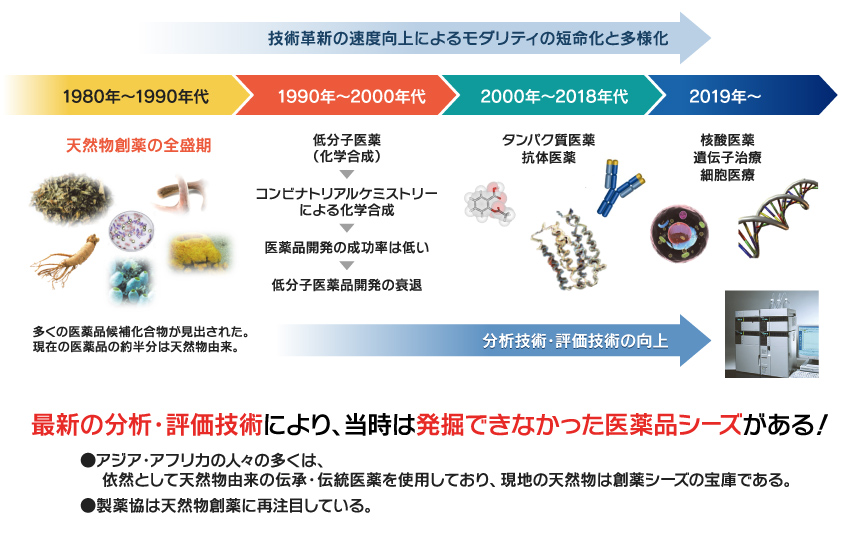
なぜ 今天然物創薬か センター紹介 熊本大学大学院生命科学研究部附属 グローバル天然物科学研究センター

新薬開発について Craの仕事とは 派遣 人材派遣のテンプスタッフ

無料 製薬業界の現状と新薬開発の流れ 転職セミナー 個別相談会 2 23 金 秋葉原 Peatix
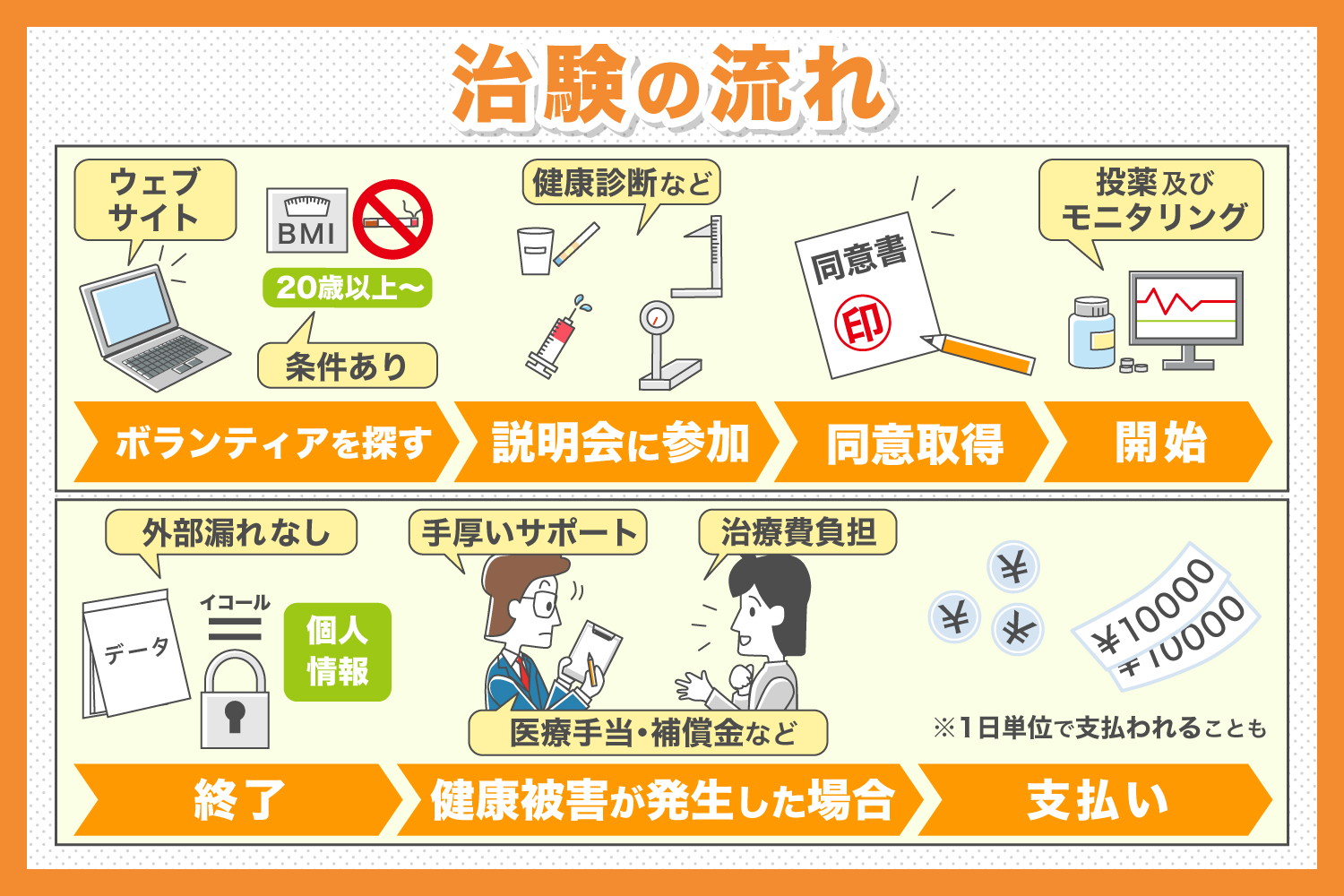
治験に興味ある方必見 応募の流れを解説します 治験モニターのススメ

ファルマバレーセンター 新薬開発の流れ
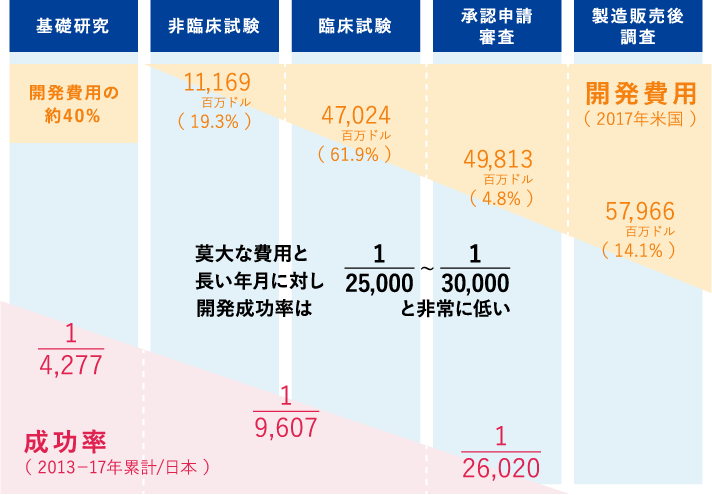
くすりができるまで 採用サイト エイツーヘルスケア株式会社
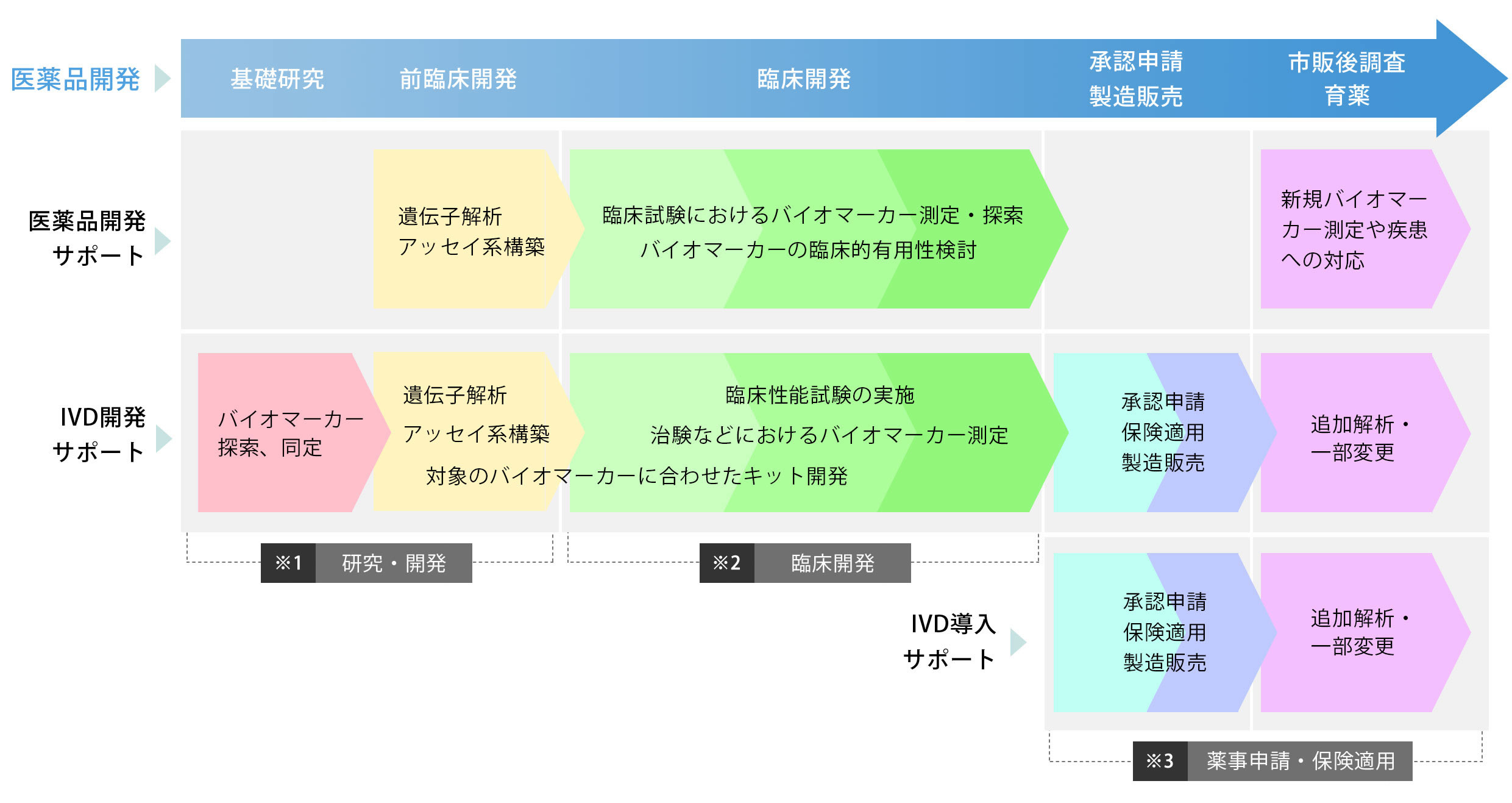
医薬品開発支援

特集 がんに勝つ薬 免疫で戦う オプジーボ 患者に新たな選択肢提供 村上和巳 週刊エコノミスト Online

目薬ができるまで その1 創薬 Santenについて 参天製薬
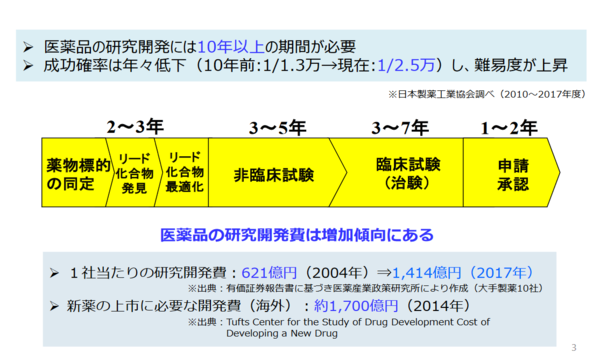
闘病記 近況について色々と 158 2019年4度目の大学病院通院 その2 封入体筋炎患者闘病記

乳がん 乳房摘出せず治療 徳島大グループが新薬開発 3年後の実用化目指す 産経ニュース

研究開発部門 部門紹介 製薬 医薬品 十全化学株式会社の求人情報
新型コロナ特効薬の開発は進むか ウイルス薬とワクチンの特許分析 日経クロステック Xtech
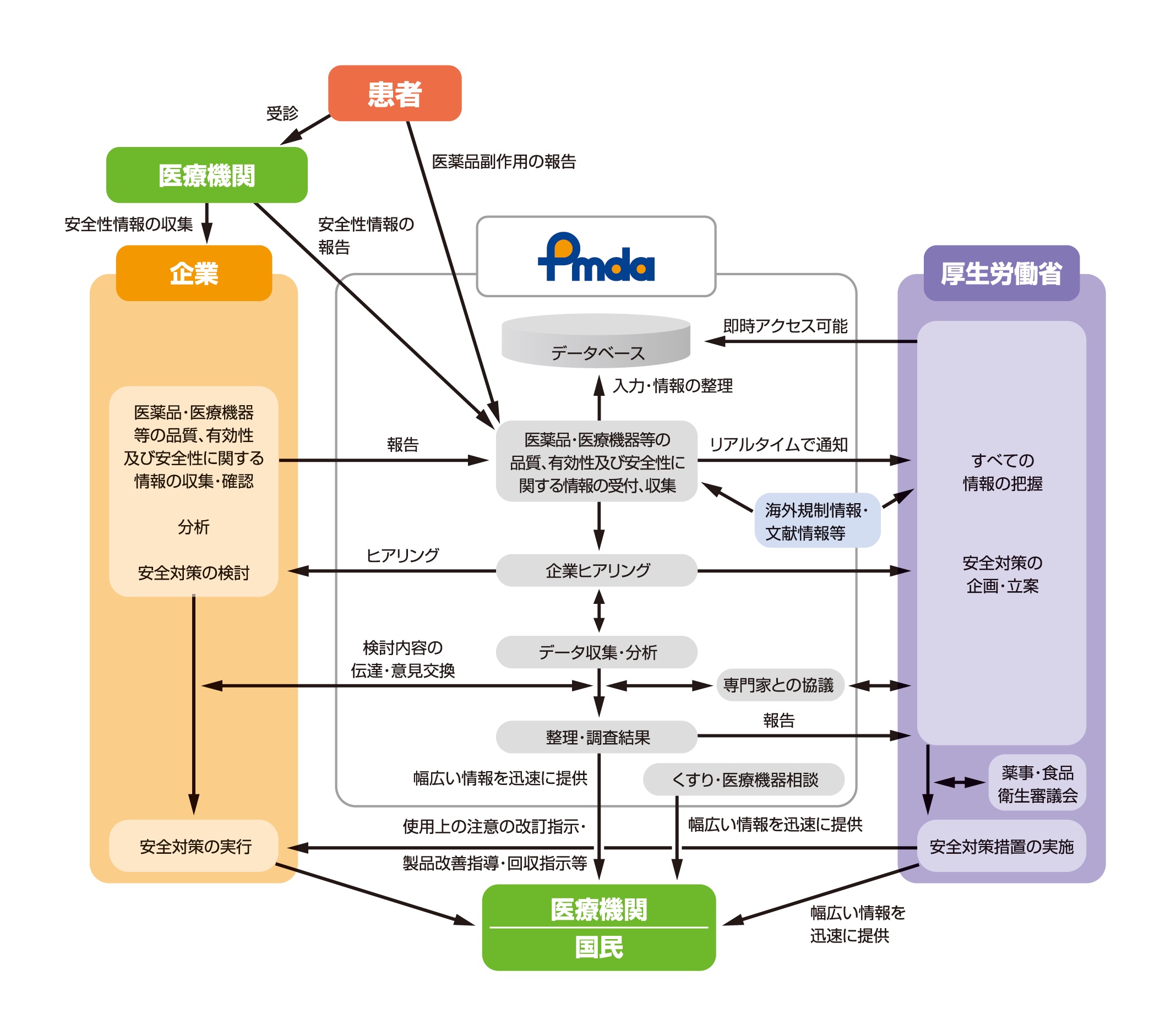
安全対策業務の概要 独立行政法人 医薬品医療機器総合機構
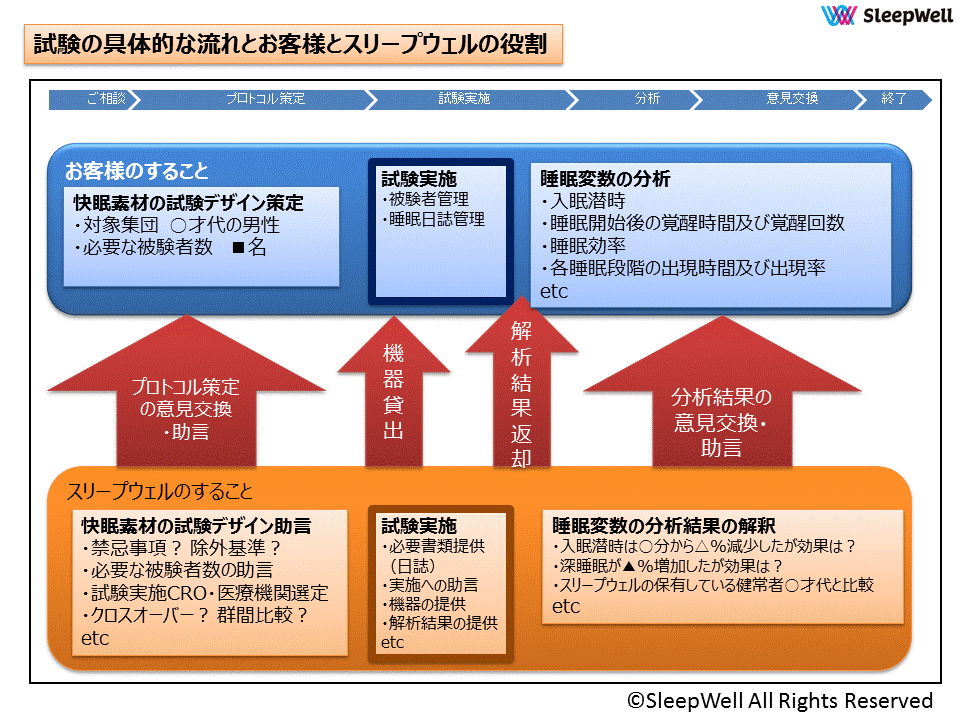
医薬品の開発支援 睡眠科学を手のひらに スリープウェル株式会社

新薬開発に欠かせないスクリーニングを劇的に効率化する手法を開発 Nedoプロジェクト実用化ドキュメント

研究開発部門 部門紹介 製薬 医薬品 十全化学株式会社の求人情報
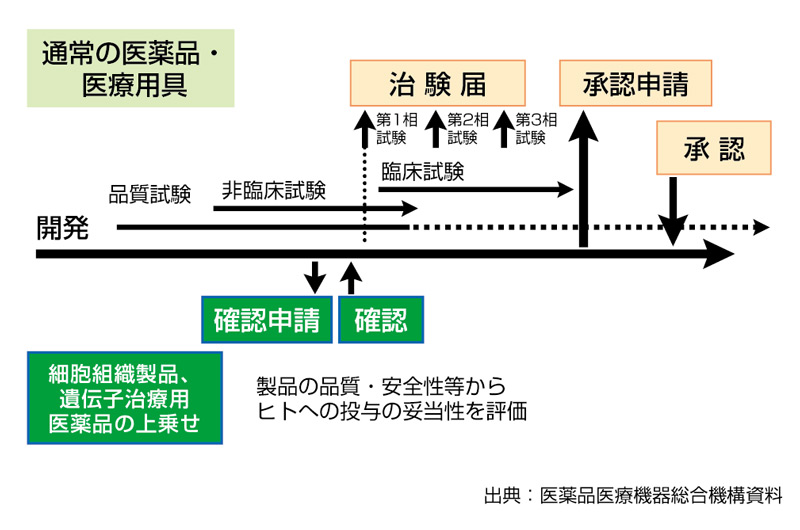
医薬品や医療機器の臨床試験や審査 承認の現場が新しい展開を迎えている 特集記事 Nature Careers Nature Research
医薬品業界の基礎知識 Eラーニング アイアール技術者教育研究所 製造業エンジニア 研究開発者のための研修 教育ソリューション

Cro Smoについて 転職クチコミ 会社 業界の評判ならキャリドア

ファルマバレーセンター 新薬開発の流れ
新型コロナ 急がれる医薬品開発 抗ウイルス薬やワクチンが なかなかできないのはなぜ ニッセイ基礎研究所
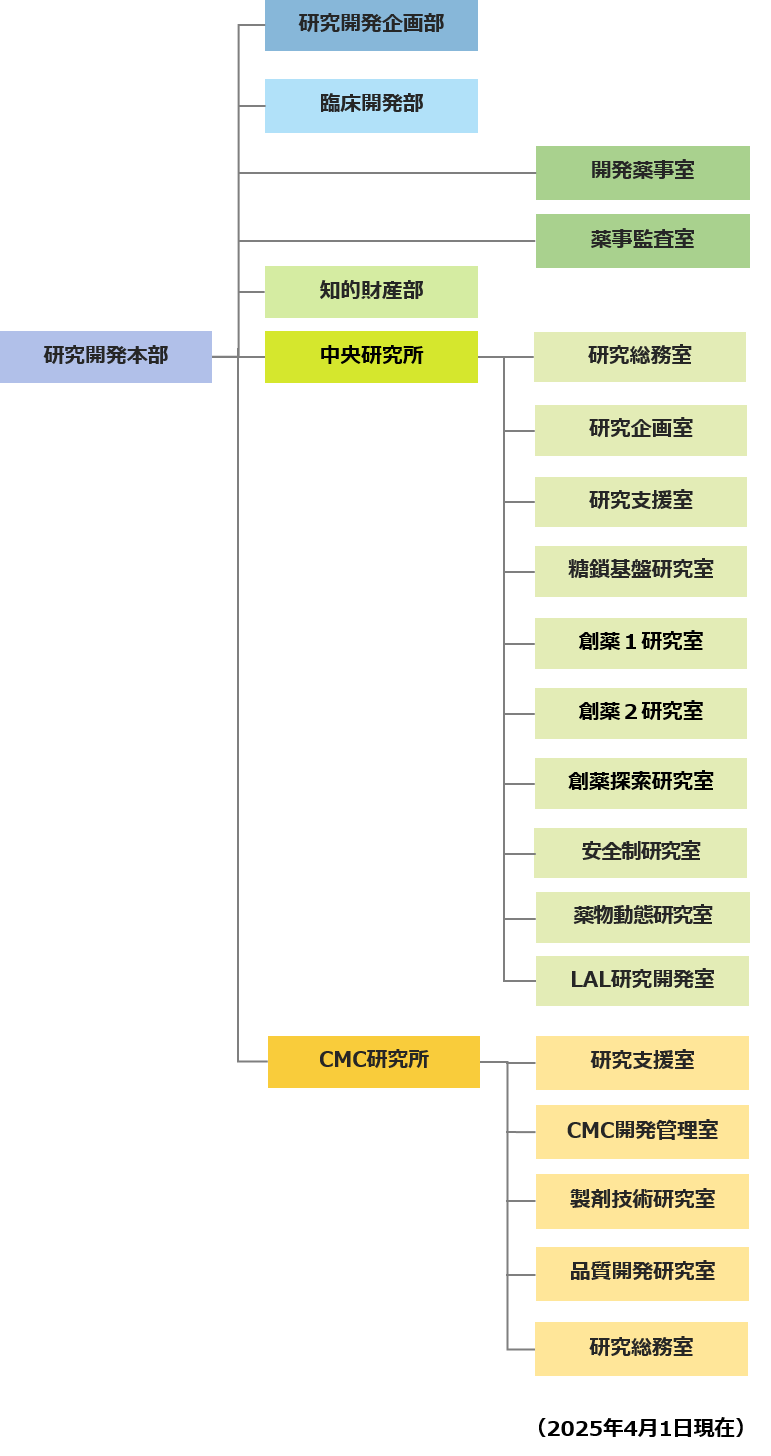
研究開発体制 研究開発 生化学工業株式会社
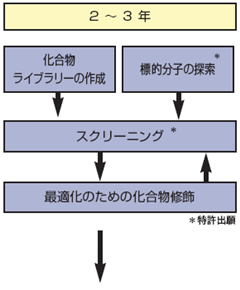
医薬品 Ii新薬の研究開発 承認のプロセス

Cro業界とcraの仕事 株式会社micメディカル
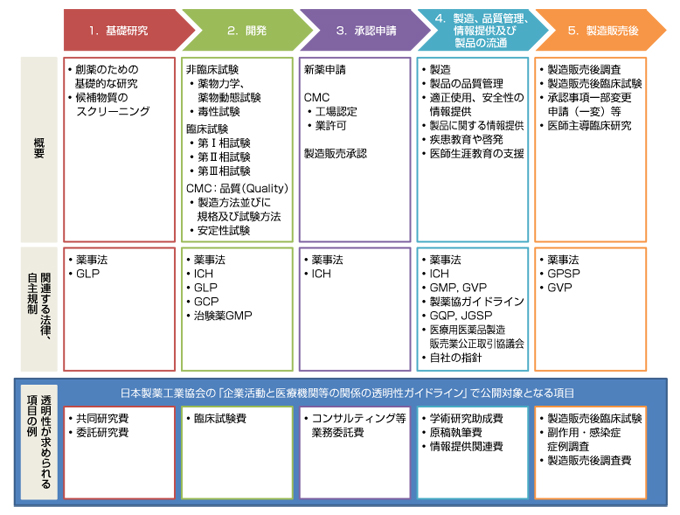
Efpia Japan くすりの一生

富士フイルム 記録紙総合サイト Club Gc
Q Tbn 3aand9gctpjrfcyzrbe3qhwwfyoijhpbyxrjnsqqwuvyqaks1fqhfurf9 Usqp Cau
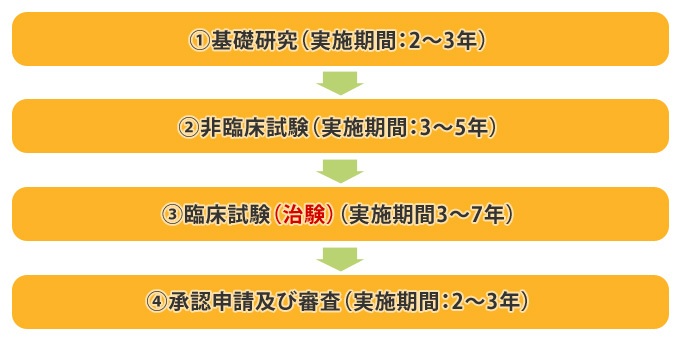
治験モニターは怖い リスクと安全性について 治験ネット
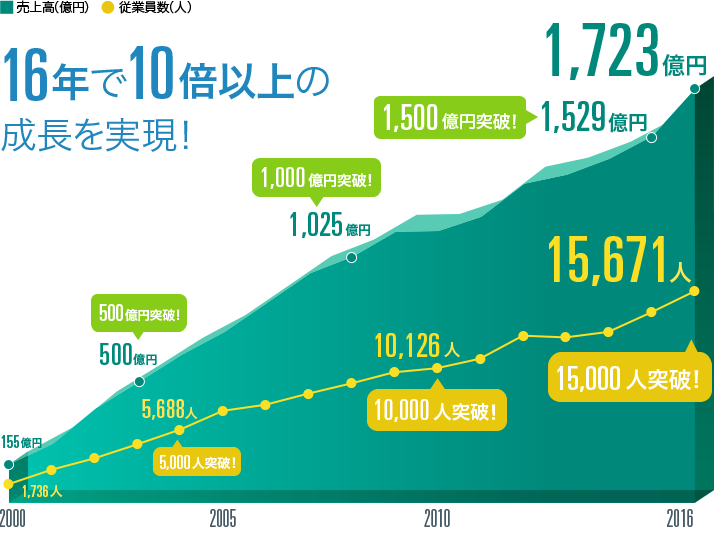
Croで働く魅力とは Croの仕事 一般社団法人 日本cro協会

ニューライフ タイムズ ジェネリック医薬品の謎
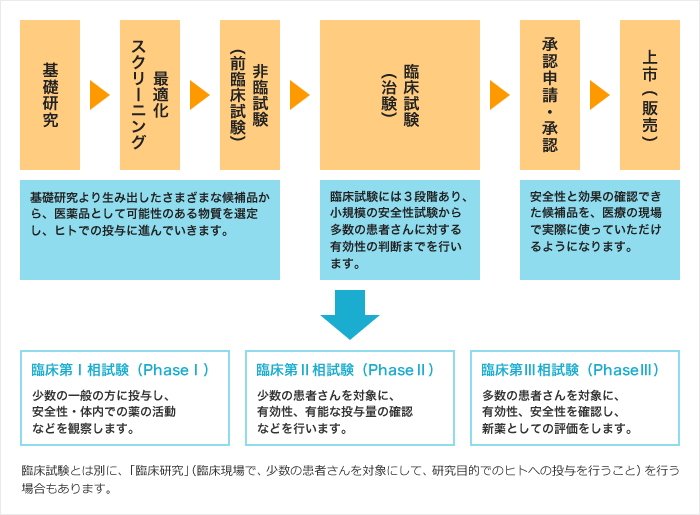
研究開発パイプライン Sbiバイオテック
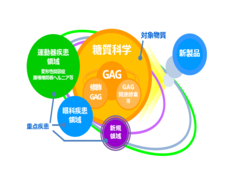
新薬研究開発のプロセス 研究開発 生化学工業株式会社
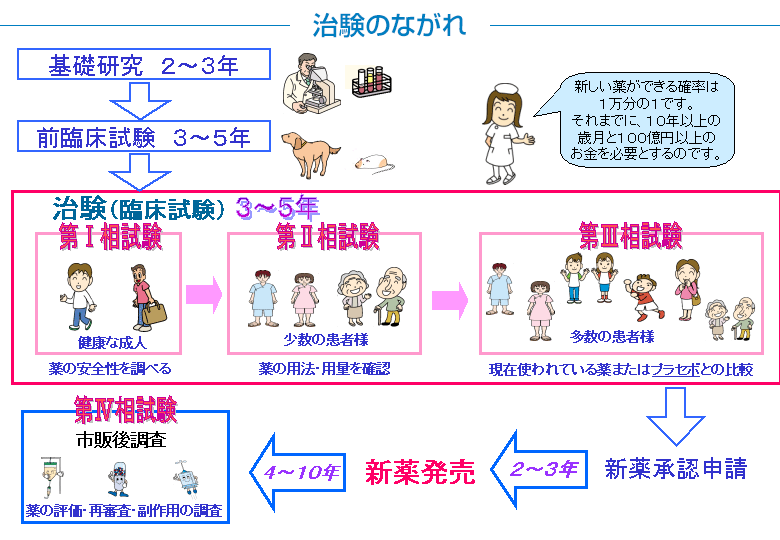
2 治験の流れ 旭川医科大学 臨床研究支援センター

Covid 19のワクチンと治療薬はいつできる Di Online

事業について 株式会社リニカル
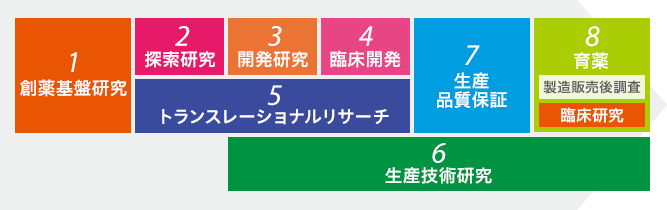
研究開発について 研究開発 協和キリン

医薬品メーカーへの就職と業界動向 薬剤師 薬学部生の新卒採用 就職 求人情報ならめでぃしーんねっと21
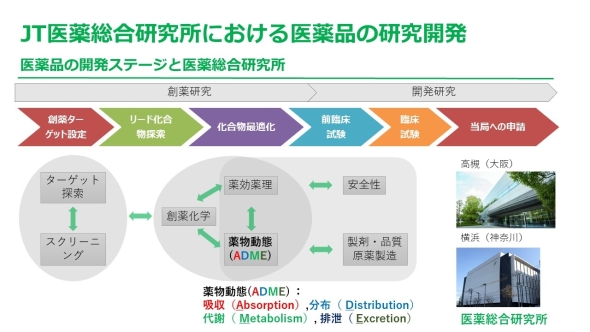
1万種類もの化合物を合成する新薬開発 データ管理が開発効率化の決め手に Monoist
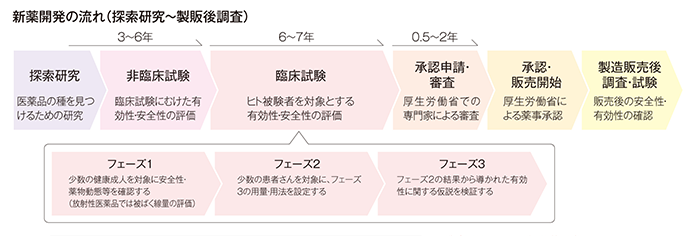
研究開発取り組み事例 日本メジフィジックス株式会社

超巨大産業 医薬品業界 で進む変革水平分業化の進展でイノベーション創出が加速 ものづくり未来図 日経bp総研
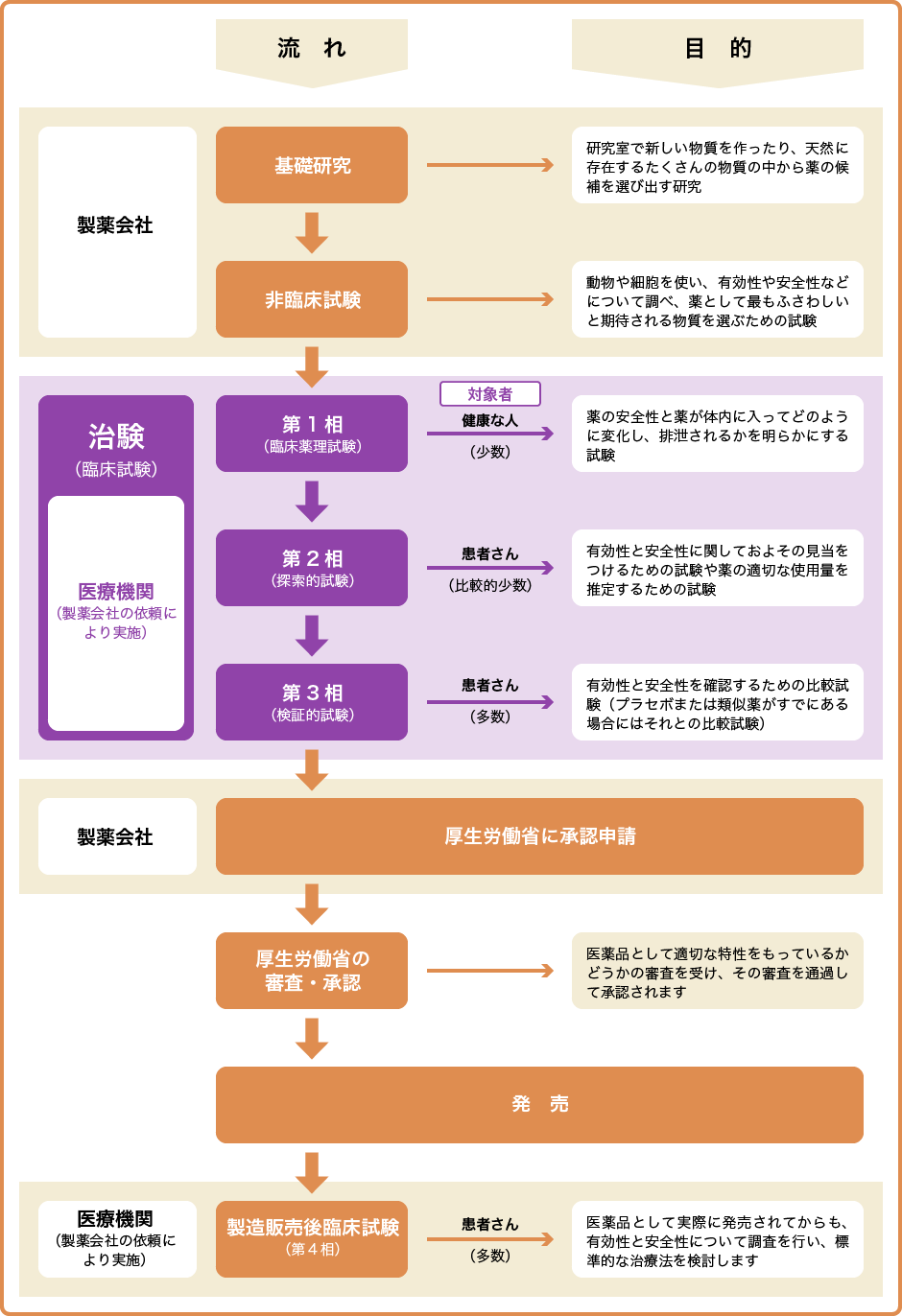
臨床研究 治験とは 一般の方へ 臨床研究管理センター Center For Clinical Research 富山大学附属病院
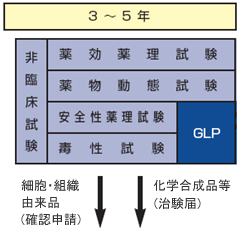
医薬品 Ii新薬の研究開発 承認のプロセス
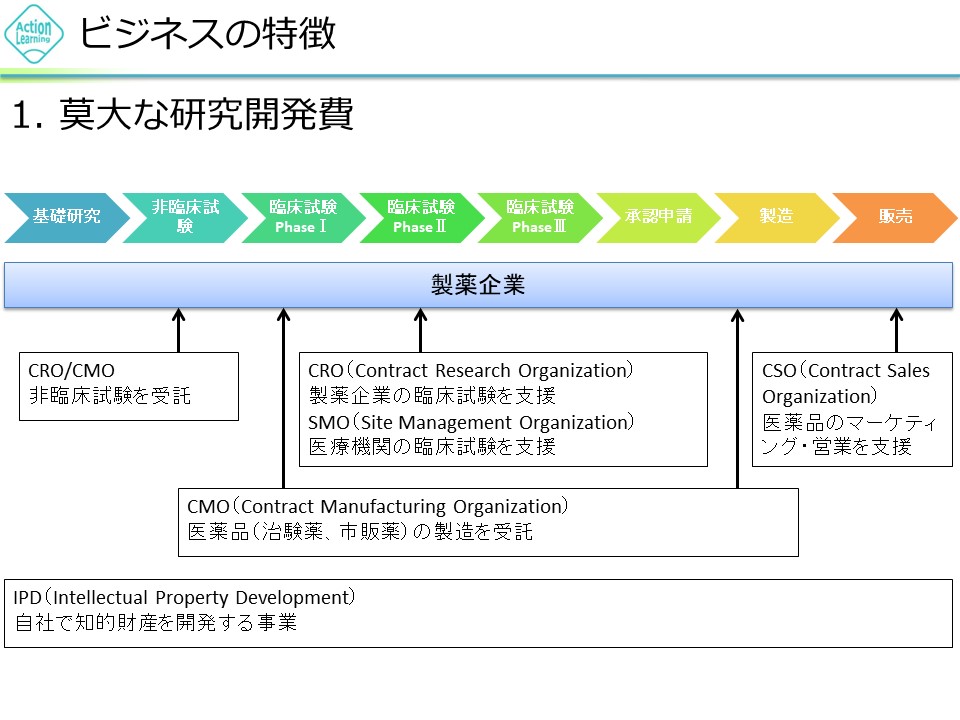
新薬メーカー業界研究 の解説 バリュートレンド 長期投資家のためのir情報

承認審査業務 申請 審査等 独立行政法人 医薬品医療機器総合機構



